Explorando las proteínas y ácidos nucleicos
Bioquímica: Moléculas de la Vida
Explorando las proteínas y ácidos nucleicos
Bienvenidos al Mundo de la Bioquímica
La bioquímica es la ciencia que estudia los procesos químicos que ocurren en los seres vivos. En este recurso educativo, exploraremos dos de las macromoléculas más importantes para la vida: las proteínas y los ácidos nucleicos.

Estructura tridimensional de una proteína
Estas moléculas son esenciales para todos los procesos biológicos, desde la estructura celular hasta la transmisión de información genética. A lo largo de este material, descubrirás su composición, estructura, funciones y la importancia que tienen para la vida.
Antes de comenzar, reflexiona sobre estas preguntas:
- ¿Qué sabes actualmente sobre proteínas y ácidos nucleicos?
- ¿Dónde crees que se encuentran estas moléculas en tu cuerpo?
- ¿Por qué crees que son importantes para los seres vivos?
Toma nota de tus respuestas y compáralas con lo que aprenderás a continuación.
Proteínas: Las Máquinas Moleculares de la Vida
Las proteínas son macromoléculas esenciales para todos los seres vivos, responsables de una amplia gama de funciones biológicas. Constituyen aproximadamente el 50% del peso seco de las células y son fundamentales para la estructura, función y regulación de los tejidos y órganos.
Aminoácidos: Los Bloques Constructores
Las proteínas están formadas por cadenas lineales de aminoácidos, unidos mediante enlaces peptídicos. Existen 20 aminoácidos proteinogénicos estándar que se encuentran en las proteínas de la mayoría de los organismos.

Estructura básica de un aminoácido genérico
Cada aminoácido tiene una estructura común que consiste en:
- Un grupo amino (-NH₂)
- Un grupo carboxilo (-COOH)
- Un átomo de hidrógeno (-H)
- Una cadena lateral (grupo R) que determina las propiedades específicas de cada aminoácido
Los aminoácidos se clasifican según las propiedades de sus cadenas laterales en:
- Aminoácidos no polares: Alanina, Valina, Leucina, Isoleucina, Prolina, Fenilalanina, Triptófano, Metionina
- Aminoácidos polares sin carga: Glicina, Serina, Treonina, Cisteína, Tirosina, Asparagina, Glutamina
- Aminoácidos ácidos: Ácido aspártico, Ácido glutámico
- Aminoácidos básicos: Lisina, Arginina, Histidina
Enlace Peptídico y Clasificación de las Proteínas
El enlace peptídico se forma mediante una reacción de condensación entre el grupo amino de un aminoácido y el grupo carboxilo de otro, liberando una molécula de agua. Esta unión es covalente y relativamente estable.

Modelo de bolas y palos de un péptido
Las proteínas se pueden clasificar de diversas formas:
Por su composición:
- Proteínas simples: Formadas únicamente por aminoácidos (ej. albúmina)
- Proteínas conjugadas: Contienen además un componente no proteico llamado grupo prostético (ej. hemoglobina con grupo hemo)
Por su estructura:
- Estructura primaria: Secuencia lineal de aminoácidos
- Estructura secundaria: Patrones locales como α-hélices y láminas β
- Estructura terciaria: Plegamiento tridimensional de toda la cadena
- Estructura cuaternaria: Asociación de varias cadenas polipeptídicas

Estructura de una α-hélice

Estructura de una hoja β plegada

Colágeno (estructura triple hélice)

Estructura de la hemoglobina
Por su función:
- Enzimas: Catalizan reacciones bioquímicas
- Estructurales: Proporcionan soporte (ej. colágeno, queratina)
- Transportadoras: Mueven moléculas (ej. hemoglobina)
- Contráctiles: Permiten el movimiento (ej. actina, miosina)
- Defensivas: Protegen contra patógenos (ej. anticuerpos)
- Reguladoras: Controlan procesos fisiológicos (ej. hormonas)
- Reserva: Almacenan nutrientes (ej. ovoalbúmina)

Suero de leche en polvo, una fuente común de proteínas
Enzimas y Vitaminas
Las enzimas son proteínas especializadas que actúan como catalizadores biológicos, acelerando las reacciones químicas en los sistemas vivos sin consumirse en el proceso. Su funcionamiento se explica mediante el modelo de llave-cerradura o el modelo de ajuste inducido.
La enzima amilasa salivar, presente en la saliva, cataliza la hidrólisis del almidón en maltosa durante la digestión. Sin esta enzima, la descomposición del almidón sería extremadamente lenta a temperatura corporal.
Las vitaminas son compuestos orgánicos esenciales que el organismo necesita en pequeñas cantidades para funcionar correctamente. Muchas vitaminas actúan como coenzimas o precursores de coenzimas, ayudando a las enzimas en sus funciones catalíticas.
- Vitamina B1 (Tiamina): Coenzima en el metabolismo energético
- Vitamina B2 (Riboflavina): Componente de FAD y FMN, coenzimas en reacciones redox
- Vitamina B3 (Niacina): Componente de NAD+ y NADP+, coenzimas en reacciones redox
- Vitamina B6 (Piridoxina): Coenzima en el metabolismo de aminoácidos
Estructura y Desnaturalización de las Proteínas
La estructura tridimensional de una proteína es crucial para su función. Esta estructura está determinada por la secuencia de aminoácidos (estructura primaria) y se mantiene mediante diferentes tipos de interacciones:
- Enlaces de hidrógeno: Entre grupos polares
- Interacciones hidrofóbicas: Entre cadenas laterales no polares
- Puentes salinos: Entre grupos con carga opuesta
- Fuerzas de van der Waals: Entre átomos cercanos
- Enlaces disulfuro: Entre residuos de cisteína (covalentes)
La desnaturalización es el proceso por el cual una proteína pierde su estructura tridimensional nativa, y por lo tanto su función, debido a la ruptura de las interacciones que mantienen su estructura, sin afectar los enlaces peptídicos. Los agentes desnaturalizantes incluyen:
- Calor: Aumenta la agitación térmica, rompiendo interacciones débiles
- Cambios de pH: Alteran los estados de ionización de los grupos cargados
- Solventes orgánicos: Alteran las interacciones hidrofóbicas
- Agentes reductores: Rompen los puentes disulfuro
- Detergentes: Interfieren con las interacciones hidrofóbicas
Cuando cocinamos un huevo, la clara (que contiene principalmente ovoalbúmina) pasa de ser transparente y líquida a opaca y sólida. Este cambio se debe a la desnaturalización de las proteínas por el calor, que altera su estructura terciaria.
Para consolidar tu conocimiento sobre proteínas, realiza las siguientes actividades:
- Investiga tres enfermedades humanas causadas por alteraciones en la estructura de proteínas y explica brevemente cada una.
- Diseña un experimento sencillo para demostrar la desnaturalización de proteínas usando clara de huevo.
- Identifica en tu dieta diaria al menos cinco fuentes diferentes de proteínas y clasifícalas según su origen (animal o vegetal) y calidad biológica.
Las proteínas son verdaderamente las moléculas de la vida, realizando una asombrosa variedad de funciones que hacen posible la existencia de los seres vivos. Su estudio continúa revelando nuevos aspectos de su complejidad y versatilidad, con aplicaciones en medicina, biotecnología y nutrición.
Ácidos Nucleicos: Los Archivos de la Vida
Los ácidos nucleicos son macromoléculas biológicas esenciales para almacenar, transmitir y expresar la información genética en todos los seres vivos. Existen dos tipos principales: el ácido desoxirribonucleico (ADN) y el ácido ribonucleico (ARN).

La doble hélice del ADN, icono de la biología molecular
Nucleótidos y Sus Funciones
Los nucleótidos son las unidades monoméricas que constituyen los ácidos nucleicos. Cada nucleótido está formado por tres componentes:
- Una base nitrogenada: Puede ser púrica (adenina, guanina) o pirimidínica (citosina, timina en ADN, uracilo en ARN)
- Un azúcar pentosa: Desoxirribosa en el ADN y ribosa en el ARN
- Uno o más grupos fosfato: Proporcionan carga negativa y participan en la formación de enlaces

Estructura molecular de un nucleótido de ADN
Los nucleótidos no solo son los bloques constructores de los ácidos nucleicos, sino que también desempeñan otras funciones cruciales en la célula:
- ATP (adenosín trifosfato): Principal molécula de transferencia de energía en las células
- GTP (guanosín trifosfato): Participa en la síntesis de proteínas y en la transducción de señales
- AMP cíclico (cAMP): Importante segundo mensajero en vías de señalización celular
- NAD+ y FAD: Coenzimas en reacciones de oxidación-reducción
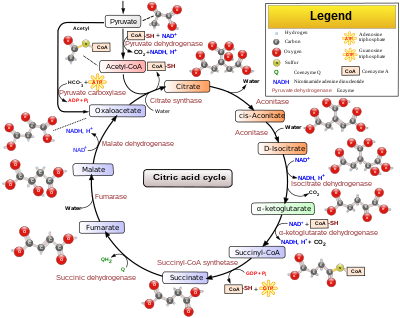
- Coenzima A: Esencial en el metabolismo de ácidos grasos y el ciclo de Krebs
El ATP actúa como "moneda energética" celular. Cuando se hidroliza a ADP, libera energía que impulsa procesos como la contracción muscular, el transporte activo a través de membranas y la síntesis de macromoléculas.
Composición y Estructura
Los ácidos nucleicos son polímeros formados por la unión de nucleótidos mediante enlaces fosfodiéster entre el grupo hidroxilo en el carbono 3' de un nucleótido y el grupo fosfato en el carbono 5' del siguiente nucleótido. Esta unión crece en dirección 5'→3'.

Diferencias estructurales entre ADN y ARN
Estructura del ADN:
El ADN está formado por dos cadenas antiparalelas (una en dirección 5'→3' y la otra en dirección 3'→5') que se enrollan formando una doble hélice. Las bases nitrogenadas se orientan hacia el interior de la hélice, donde forman pares de bases complementarias:
- Adenina (A) se aparea con Timina (T) mediante dos enlaces de hidrógeno
- Guanina (G) se aparea con Citosina (C) mediante tres enlaces de hidrógeno

Esquema de la replicación del ADN
La estructura del ADN fue elucidada por James Watson y Francis Crick en 1953, basándose en los trabajos de Rosalind Franklin y Maurice Wilkins. Esta estructura en doble hélice explica cómo el ADN puede replicarse y transmitir información genética.
Estructura del ARN:
A diferencia del ADN, el ARN generalmente es monocatenario (de una sola cadena), aunque puede formar estructuras secundarias complejas mediante apareamiento de bases intramolecular. Existen varios tipos de ARN con funciones específicas:
- ARN mensajero (ARNm): Transporta la información genética desde el ADN hasta los ribosomas para la síntesis de proteínas
- ARN de transferencia (ARNt): Lleva aminoácidos específicos al ribosoma durante la síntesis proteica
- ARN ribosomal (ARNr): Componente estructural y catalítico de los ribosomas
- ARN pequeños: Diversos tipos como microARN, ARN de interferencia, etc., que regulan la expresión génica

Estructura de un ARN de transferencia (tRNA)

Esquema del proceso de transcripción (ADN a ARN)

Ribosoma sintetizando una proteína durante el proceso de traducción
Las diferencias químicas entre ADN y ARN incluyen:
- El azúcar en el ADN es desoxirribosa (sin grupo OH en el carbono 2'), mientras que en el ARN es ribosa (con grupo OH en el carbono 2')
- El ADN contiene timina, mientras que el ARN contiene uracilo
- El ADN es generalmente bicatenario, mientras que el ARN es generalmente monocatenario
- El ADN es más estable químicamente que el ARN
El dogma central de la biología molecular describe el flujo de información genética: ADN → ARN → Proteína. Esto significa que la información contenida en el ADN se transcribe a ARN mensajero, que a su vez se traduce a una secuencia específica de aminoácidos para formar una proteína funcional.
La estructura de los ácidos nucleicos no se limita a la simple secuencia lineal de nucleótidos. Tanto el ADN como el ARN pueden adoptar estructuras tridimensionales complejas que son esenciales para sus funciones:
- Superenrollamiento: El ADN en las células está superenrollado, lo que permite el empaquetamiento en espacios reducidos y regula la accesibilidad para la transcripción
- Estructuras terciarias de ARN: Como el brazo aceptor y el brazo anticodón en el ARNt, o las estructuras de horquilla en otros ARN
- Complejos proteína-ácido nucleico: Como los nucleosomas (ADN + histonas) o los ribosomas (ARNr + proteínas)
Para profundizar en tu comprensión de los ácidos nucleicos, realiza las siguientes actividades:
- Investiga y explica el experimento de Griffith y el de Hershey-Chase, que demostraron que el ADN es el material genético.
- Construye un modelo físico de la doble hélice del ADN usando materiales sencillos (como cartón, palillos o materiales reciclados).
- Analiza cómo las mutaciones en la secuencia de nucleótidos del ADN pueden afectar la estructura y función de las proteínas resultantes.
Los ácidos nucleicos son la base molecular de la herencia y la diversidad biológica. Su estudio ha revolucionado nuestra comprensión de la vida y ha dado lugar a avances extraordinarios en medicina, agricultura y biotecnología. Desde la terapia génica hasta la edición del genoma con tecnologías como CRISPR, el conocimiento de los ácidos nucleicos continúa transformando nuestra capacidad para entender y manipular los procesos de la vida.